近日,我院劳动卫生与环境卫生系郑玉新教授和晋小婷教授团队在新型阻燃剂磷酸三(2-氯乙基)酯(TCEP)心脏损伤效应及机制研究方面取得重要成果。相关研究成果以“Cardiotoxicity of tris(2-chloroethyl) phosphate exposure: Insights into the role of oxygen sensor mediated energy metabolism remodeling”为题发表于国际学术期刊Journal of hazardous materials上(影响因子12.2,DOI:10.1016/j.jhazmat.2025.137113)。
阻燃剂在锂电池电解液中扮演着至关重要的角色,能够显著提升电池的安全性能。其中,有机磷系阻燃剂(OPFRs)因其优异的电化学稳定性、环保特性、成本效益及高效的阻燃能力,在锂电池行业中得到广泛应用。磷酸三(2-氯乙基)酯(TCEP)作为一种新型高效的含磷阻燃剂,不仅广泛应用于锂电池领域,还被大量用于家具、建筑材料等行业。然而,TCEP的非共价结合特性使其易于进入环境,导致其在空气、水源及食物链中广泛分布,环境暴露风险日益增加。研究表明,中国人群日均TCEP摄入量可达96.9至46,700纳克/千克体重,接近安全参考剂量(7000纳克/千克体重)。因此,TCEP的健康风险备受关注。此前研究已发现TCEP对生殖系统和神经系统具有毒性,但关于其对心脏的影响及其机制尚不明确。心血管疾病是全球范围内发病和死亡的首要原因,因此,探究TCEP对心脏的毒性效应及其机制具有重要的科学意义和公共卫生价值。
本研究通过建立TCEP暴露小鼠模型,系统评估了TCEP对心脏的毒性效应及其分子机制。研究发现,低剂量TCEP暴露即可引发心脏损伤。连续36天暴露于70-700微克/千克体重TCEP的小鼠(相当于人类安全参考剂量的1-10倍)出现心室扩张、心肌细胞肥大、心电异常以及心肌缺氧和损伤状态。这一发现提示,当前TCEP的安全阈值可能需要重新评估,尤其需要关注食品和环境中长期低剂量暴露的潜在风险。进一步代谢组学分析显示,TCEP暴露诱导心脏能量代谢从“有氧代谢”向“无氧代谢”转变,导致ATP生成减少和乳酸堆积,从而加剧心肌损伤。实验证实,通过激活氧化磷酸化(如EGCG)或抑制糖酵解(如2-DG)可逆转TCEP诱导的心脏损伤,这为开发针对阻燃剂毒性的保护性药物提供了潜在靶点。在机制研究方面,团队围绕氧感受器调控的能量代谢途径,发现TCEP通过促进氧感受器PHD2蛋白的泛素化降解,抑制其正常功能,导致缺氧诱导因子HIF-1α异常积累。HIF-1α入核后驱动糖酵解相关基因表达,最终引发能量代谢重塑和心脏功能障碍。这一研究首次阐明了TCEP通过氧传感器PHD2-HIF-1α轴调控能量代谢的分子路径,为阻燃剂毒性机制研究开辟了新的方向。
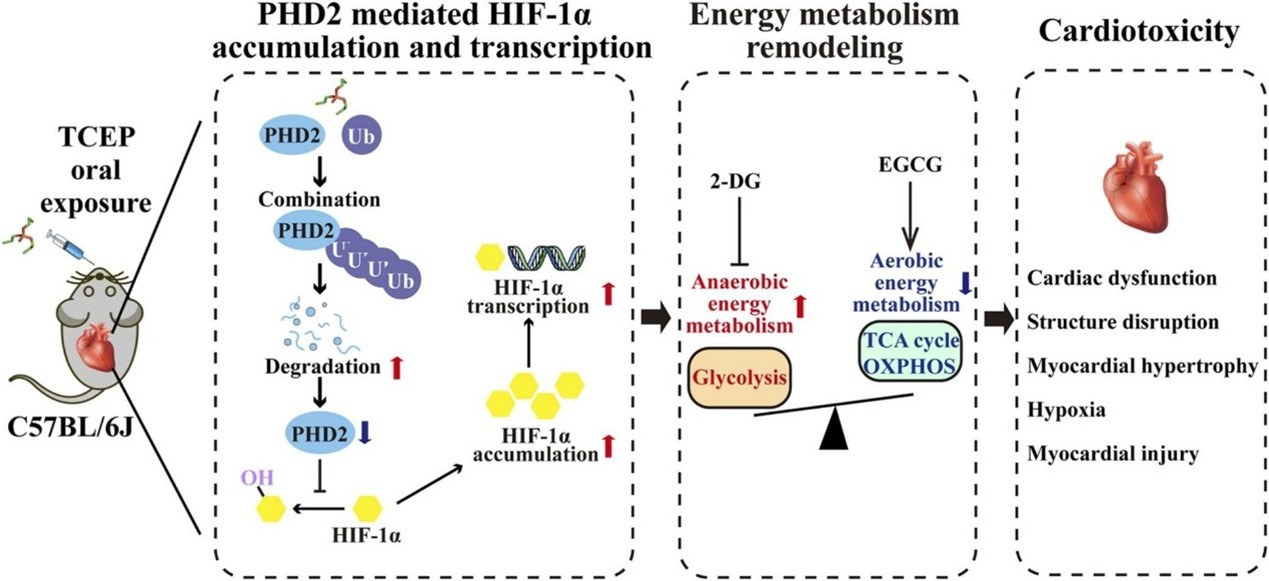
图:TCEP暴露通过诱导氧感受器PHD2蛋白降解致HIF-1α异常积累调控心肌能量代谢重塑诱导心肌损伤(图片来自DOI:10.1016/j.jhazmat.2025.137113)
本研究不仅揭示了TCEP暴露对心脏的毒性效应及其分子机制,还为阻燃剂的环境健康风险评估提供了重要的科学依据。研究结果表明,当前TCEP的安全阈值可能需要重新评估,尤其是在长期低剂量暴露的情况下。此外,研究发现的能量代谢重塑机制为开发针对阻燃剂毒性的干预策略提供了潜在靶点,具有重要的临床应用前景。
青岛大学郑玉新教授和晋小婷教授为本文通讯作者,研究生张泽和郑楚儿为本文共同第一作者。本研究合作单位包括中国疾病预防控制中心职业卫生与中毒控制所以及University of Karachi。该研究得到国家自然科学基金(No. 82241086,82473674),青岛自然科学基金(24-4-4-zrjj-157-jch)和山东省泰山青年学者基金(tsqn201909101)的支持。